DOSAGE CONDUCTIMÉTRIQUE
d'un ACIDE ou d'une BASE forte
![]()
I Objectifs
II Acquisitions et transfert
III Étude de l'équivalence
IV Application: dosage d'une solution
commerciale acide ou basique forte
![]()
I Objectifs
|
 |
II Acquisitions et transfert
A. Étude choisie et principe du dosage
Pour déterminer par exemple la concentration d'une solution de soude, on la dose au moyen d'une solution d'acide chlorhydrique de concentration connue, en effectuant un suivi conductimétrique: on mesure la conductivité s (conductance G) au fur et à mesure du dosage, et on repère son minimum pour déterminer l'équivalence; puis on calcule la concentration initiale de la solution basique à partir de l'équivalence.
B. Matériels et montage
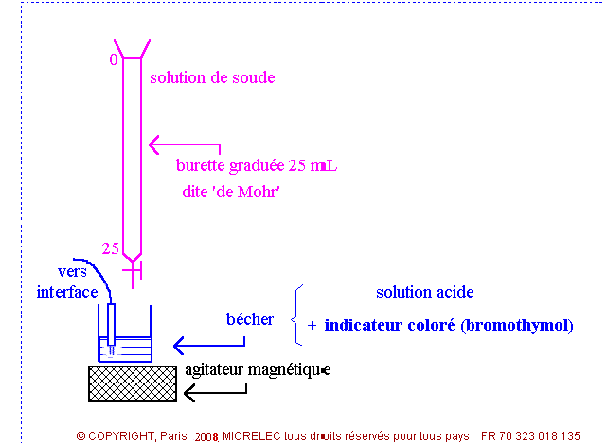
1. Le montage
C'est le même montage que celui utilisé traditionnellement pour un suivi pH métrique de dosage:
2. Le nouveau capteur conductimétrique DB15 (réf M12P307) à reconnaissance automatique
 |
|
Penser à brancher les haut-parleurs! |
Mise en oeuvre:
 |
(1) Ouvrir le logiciel
d'acquisition
(2) Brancher la prise DB15 du capteur sur l'une des prises G, H, etc. d'ORPHY (3) Le logiciel détecte instantanément le capteur et met à jour l'écran: |
|
3. L'ancien capteur conductimétrique à prise DIN 6 broches
consulter la fiche technique du capteur Micrelec
L'électrode de mesures est celle du conductimètre Micrelec (sinon, il faudra procéder à son étalonnage préalable). Ce module doit être relié à la prise F d'Orphy, ce qui assure son alimentation en ± 12 V, en même temps que la mesure analogique de la conductivité s (ou de la conductance G) sur l'entrée EA2.
|
|
NB: sur ORPHY GTI2, les prises DIN 6 broches repérées A à F n'existent plus: il suffit alors de brancher l'adaptateur DIN pour GTI2 réf M12G504 pour disposer de ces prises (sur lesquelles se branche le module Transel, l'ancien module de pression, etc). |
C. Protocole expérimental et préparation
On utilisera par exemple des solutions centimolaires (0.01 mol/L)pour l'acide et la base.
1. Préparation de la solution acide du bécher de dosage:Prélever (pipette 10mL) la quantité d'acide chlorhydrique 0.01 M nécessaire au dosage, et la déposer dans le bécher. Puis ajouter:
|

|
2. Préparation de la solution basique de la burette graduée
Une solution de soude (voisine de 0.01 M) est placée dans la burette graduée, et le zéro ajusté soigneusement.
D. Réglages logiciels
Soit Vb le volume total de soude versé (= 'chute de burette') à un instant quelconque dans l'acide. On mesure la conductivité s (conductance G) au fur et à mesure de l'ajout de soude.
Pour la configuration de EA2, le plus simple est de choisir le conductimètre dans la liste des capteurs proposée par le logiciel d'acquisition.
| Abscisse: |
Voies actives: |
Enregistrement: |
Acquisition: |
||||
|
clavier Vb (mL) |
EAx: |
Variable: |
Signe: |
Cal: |
Unité: |
|
|
|
EA2 |
s |
+ |
2 |
mS/cm |
|||
Charger l'acquisition pré réglée:
| * avec ORPHY-GTS2 | * avec ORPHY-GTI2 |
E. Étalonnage du conductimètre
N.B.: Conductance et conductivité sont proportionnelles (G=k*
s, avec la constante de cellule). C'est la valeur de cette constante qui est ajustée par le réglage de la vis du capteur conductimétrique. Pour des dosages, on peut indifféremment raisonner sur G ou s, puisqu'on étudie le minimum de la courbe tracée. Mais l'étalonnage se faisant à partir de tables de conductivité, on est obligé alors d'utiliser celle-ci.
|
|
F. Protocole d'acquisition
Il s'agit ici de saisir la conductivité s (conductance G) en fonction du volume Vb de base qui a chuté de la burette.
|
Chaque validation (touche "Entrée") provoque simultanément l'acquisition de la valeur courante de G et de celle de Vb (à inscrire dans la case de saisie en haut de la fenêtre logicielle) | |
|
taper d'abord la valeur 0 sur le clavier, et valider, pour acquérir la valeur initiale de la conductivité (conductance) de la solution acide | |
|
procéder à une chute de burette de 1 mL, et acquérir le point | |
|
continuer de verser la soude mL par mL jusqu'à Vb=8 mL, puis par 0.5 mL , et même goutte par goutte pour Vb proche de 10 mL; observer le minimum de s signalant le passage par l'équivalence (penser à noter en quel point le bromothymol change de couleur) | |
|
arrêter pour un volume total Vb versé de 20 à 25 mL. |
G. Variables transférées
Ä
Vb et sDans la fenêtre 'Graphiques' (menu Fenêtre/graphe Variables), vérifier qu'on a bien s= f(Vb), sinon cliquer-D pour choisir 'Coordonnées' dans le menu contextuel, ou cliquer-G sur l'icône correspondante
pour choisir:
| Vb en abscisses | |
| s en ordonnées (à gauche). |
Observer la régularité de la courbe obtenue; on peut éliminer éventuellement des points erronés (résultant d'une erreur de saisie ou d'une erreur de lecture de Vb):
| en opérant directement sur le graphe: cliquer-G sur le point incriminé, qui apparaît alors grossi, et appuyer sur la touche 'Suppr' (la visibilité des points sera facilitée en demandant dans les options graphiques les points seuls pour le tracé, i.e. sans ligne) | |
| ou sur le tableau des valeurs: sélectionner la
cellule ou la ligne
concernée puis appuyer sur le bouton
|
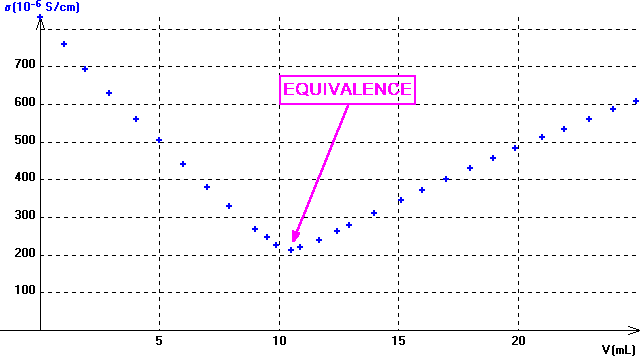
III Étude de l'équivalence
A. Modélisations |

|
| Dans la fenêtre 'Graphiques', clic-D pour choisir 'Modélisation' dans le
menu contextuel, ou touche F9, ou clic-G sur l'icône correspondante |
s=a*Vb+b
| Demander au logiciel d'ajuster (clic-G sur le bouton
"Ajuster" | |
| Répéter toutes ces opérations pour l'autre partie de la courbe. |
A ce stade, pour sauver ces informations, le graphique peut
être imprimé, ou copié dans le presse-papiers (clic-D / Copier
dans presse-papiers, ou clic-G sur le bouton ![]() )
pour être importé dans un traitement de texte.
)
pour être importé dans un traitement de texte.
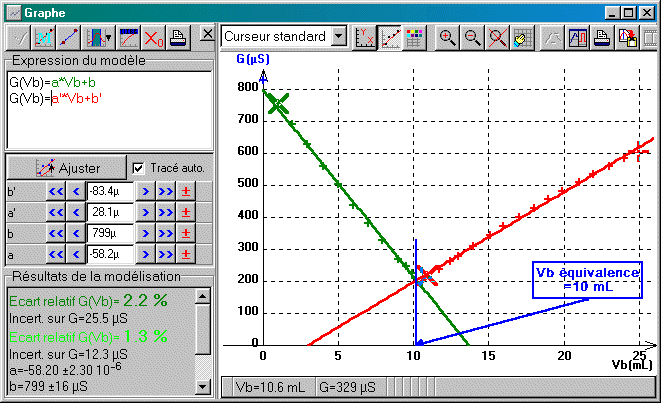
charger
le fichier Regressi
(et faire F9 pour accéder à la modélisation)
B. Détermination de la concentration de la solution de soude
L'abscisse du point d'intersection des deux droites modèles précédentes fournit le volume de base Vbé versé à l'équivalence, ce qui permet d'en déduire cB:
n(OH- versé) = n(H3O+ initial)
cA*vA = cB*Vbé
Les curseurs "ligne" et "texte", appelés dans la liste déroulante des curseurs, permettent de légender le graphique.
IV Application: dosage d'une solution commerciale acide ou basique forte
La méthode précédente pourra être appliquée au dosage conductimétrique:
| D'une solution commerciale d'acide fort (ex: détartrant pour cafetière) par la soude | |
| D'une solution commerciale de base forte (ex: déboucheur d'évier) par l'acide chlorhydrique. |
Le produit déboucheur d'évier, par exemple, sera placé
dans le bécher et dilué au moins 100 fois, pour un dosage par une
solution d'acide chlorhydrique placée cette fois-ci dans la burette de Mohr.
Cliquer ici pour ouvrir la documentation complète de Regressi
retour sommaire chapitre en cours![]()
(1) ce que fait automatiquement le programme lors d'un clic-G sur un point du graphique
.