SUIVI de CINÉTIQUE
de RÉACTIONS CHIMIQUES
![]()
I Objectifs
II Principe de la manipulation
III Montage et réglages préliminaires
IV Protocole d'acquisition
V Étude de la loi c = f(t)
![]()
I. Objectifs
|
 |
| Déduire des mesures ou du graphique les valeurs de ces vitesses | |
| Modéliser éventuellement les variations de c = f(t) suivant les hypothèses faites sur l’ordre de la réaction. |
II. Principe de la manipulation
A. Principe
Une cinétique de réaction chimique lente est suivie par l'étude de
l'évolution de la concentration en fonction du temps de l'espèce chimique colorée
formée au cours de la réaction. Cette concentration, qui est traditionnellement suivie
au moyen de dosages volumétriques successifs, peut l'être beaucoup plus simplement par
mesure de l'absorbance du milieu réactionnel à une longueur d'onde déterminée.
Quelque soit l'appareil choisi (spectrophotomètre ou colorimètre), le principe reste le
même: on mesure le flux lumineux F transmis à travers la
solution colorée, à une certaine longueur d'onde l . La
comparaison avec la mesure obtenue (Fo) pour le
solvant seul permet d'en déduire l'absorbance pour la valeur choisie de longueur d'onde:
A = log(F0 /F)
Ces mesures peuvent être effectuées à partir d'un colorimètre (par exemple Photocolor de Micrelec), ou avec n'importe quel spectrophotomètre.
Ce type d'étude demande d'avoir déterminé préalablement pour la solution de la substance colorée étudiée:
| la longueur d'onde d'absorbance maximale, après tracé de son spectre
d'absorption (voir à ce sujet le TP correspondant),
si celle-ci n'est pas connue: |
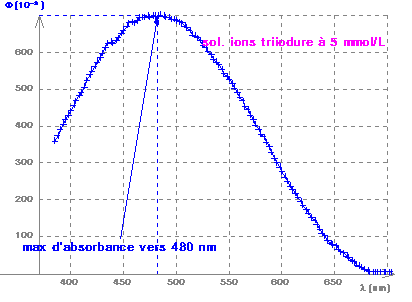 |
¬ SPECTRE
D'ABSORPTION D'UNE SOLUTION AQUEUSE D'IONS TRIIODURE DE CONCENTRATION : 5 mmol/L |
| le coefficient k de la loi de Beer-Lambert (c=k'*A ou A=k*c), à partir d'un échantillon de concentration connue de la même substance (voir aussi TP correspondant). |
B. Exemple proposé et équation de réaction
L'oxydation des ions iodure I- par l'eau oxygénée, en milieu acide, conduit à la formation d'ions tri iodure I3formation d'ions tri iodure I3- selon l'équation:2H
+ + H2O2+ 3I- ® 2H2O + I3-Ces ions colorent en brun la solution. On détermine donc son coefficient k pour la loi de Beer Lambert:
| soit en réalisant au laboratoire une solution de concentration connue c (3) et en mesurant son absorbance A | |
| soit en mélangeant les réactifs plusieurs heures, ou plusieurs jours, avant de la mesure d'absorbance: on pourra alors considérer que la vitesse de réaction est devenu quasiment nulle et qu'on a atteint la concentration maxima en produit de la réaction (à calculer à partir des données sur les réactants) |
C. Solutions utilisées: composition, concentration, volume
On peut partir des solutions suivantes dans l'eau distillée:
| Solution(A): acide sulfurique et iodure de potassium, tous deux en excès par rapport aux conditions stœchiométriques |
| Solution(B): eau oxygénée, par exemple à 0.01 mol/L. |
Les deux solutions seront utilisées par volumes égaux ou non, et avec des proportions acide/iodure variables pour (A) de façon à étudier l'influence de chaque paramètre sur la cinétique.
D. Manipulation
E. Suivi éventuel de la cinétique par dosage traditionnel
Lors d'un suivi 'classique' (sans photométrie), on effectue à intervalles de temps réguliers des prélèvements, dont on fige la composition par trempe thermique; puis on dose leurs ions tri iodure par exemple avec une solution de thiosulfate de sodium.
III. Montage et réglages préliminaires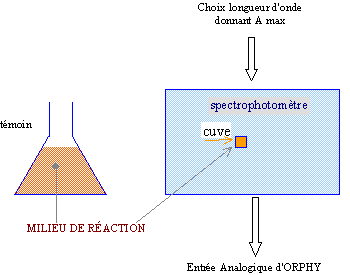
A. Liaisons et calibres
|
 |
prise B: |
prise C: |
EA4/EA5 (100 mV) |
EA6 (1 V) |
| A priori, le calibre 1 V devrait être le mieux adapté; mais les valeurs peuvent varier sensiblement d'un appareil à l'autre: c'est le "blanc" qui confirmera ou non le choix (donne la valeur la plus élevée pour la tension correspondante). | |
| une autre solution consiste à alimenter de façon autonome le module Photocolor par une pile (fournie avec), et à relier ses deux bornes de sortie par des cordons à la platine de raccordement d'ORPHY: (-) à la référence, et (+) à l'entrée analogique choisie (voir paragraphe précédent pour ce choix). |
B. Réglages des logiciels d'acquisition
Abscisse: |
Voies actives: |
Enregistrement: |
Déclenchement (synchro): |
|||||
Temps |
EAi: |
Variable: |
Signe: |
Cal: |
Unité: |
Nombre points: |
Durée: |
Manuel |
EAx |
U |
+ |
1 ou 0.1 |
V |
1 point toutes les 20 s environ ou par minute |
30 min à qqs heures |
(Clavier ou clic sur bouton) |
|
(*)
adapter si nécessaire les valeurs des bornes proposées par le logiciel à celles choisies pour l'étude du spectre. (**) acquisition automatique de A seulement si le spectrophotomètre dispose d'une sortie analogique, qui a été reliée à une entrée analogique d'Orphy. Il faut de plus avoir étalonné préalablement cette sortie analogique en déterminant le rapport entre la tension (mesurée sur la sortie) et l'absorbance lue sur l'appareil. Ce coefficient est ensuite rentré par étalonnage manuel ou interactif dans le logiciel d'acquisition.|
avec ORPHY-PORTABLE 2: brancher: capsule ±2 V, ou 0-15 V. |
Charger l'acquisition pré réglée:
| * avec ORPHY-GTS2 | * avec ORPHY-GTI |
C. Réalisation de la référence
1. avec un spectrophotomètre traditionnel
| Mettre sous tension l'appareil au moins 5 minutes avant les prises de mesures pour avoir une bonne stabilisation thermique de ses circuits | |
| Choisir sur l'échelle de réglage la longueur d'onde d'absorbance maximale de la substance à suivre (par exemple 480nm pour l'ion tri iodure de notre exemple) |
| "blanc" et optimisation du calibre utilisé: introduire dans l'orifice de l'appareil une cuve remplie au moins à moitié de la solution (A): suivre alors les indications de la notice du constructeur pour valider le blanc et passer aux mesures d'absorbance proprement dites. |
2. avec le spectrophotomètre Micrelec
Ce spectrophotomètre, piloté par le logiciel Ccdorphy, permet de tracer préalablement le spectre (par balayage automatique en longueur d'onde), puis de désigner directement sur le spectre à l'aide du pointeur la longueur d'onde à retenir dans la suite de l'étude (suivi de la cinétique). Le logiciel envoie les données à Orphy, calcule aussi l'absorbance, et permet de sauver au format Regressi les données A(l ) puis A(t) ainsi obtenues. Il permet aussi l'étude de la loi de Beer Lambert pour la détermination de k.
3. avec un colorimètre
| choisir sur le sélecteur la valeur de longueur d'onde (= une D.E.L.) la
plus proche de celle d'absorbance maximale N.B.: dans tous les cas, sélectionner la DEL et alimenter en tension le colorimètre au moins 5 minutes avant les prises de mesures pour avoir une bonne stabilisation des circuits). |
| "blanc" et optimisation du calibre utilisé: introduire dans l'orifice du colorimètre une cuve à moitié remplie de la solution (A) et fermer le volet d'obturation pour éviter l'entrée de lumière parasite: attendre quelques instants et noter la valeur de la tension de référence Uo ainsi obtenue (qui correspondra donc à une absorbance nulle). Selon les appareils, et la DEL choisie, Uo peut atteindre 100 à 150 mV. Suivant que cette valeur Uo est supérieure ou non au calibre 100 mV de l'entrée EAx, il peut y avoir lieu de changer de calibre au niveau du logiciel; mais dans tous les cas, ne laisser qu'une seule entrée analogique active pour la suite des mesures. |
A. Acquisitions
| Laisser dans l'appareil de mesures la cuve contenant la solution (A): c'est la mesure de référence c = 0 qui sera acquise à t = 0 | |
| A l'instant t = 0, mélanger les solutions (A) et (B), tout en déclenchant la première acquisition dès que la moitié d'une des solutions est versée dans l'autre (c'est donc la valeur c = 0 qui est acquise). Remplir une nouvelle cuve aux 2/3 avec ce mélange une fois homogénéisé | |
| Avant la 20è seconde, il faut avoir substitué cette cuve à celle de référence. Bien replacer le volet d'obturation dans le cas du colorimètre | |
| Les prises de mesures sont effectuées automatiquement par le logiciel pour toute la durée choisie; la partie du mélange réactionnel conservée à l'extérieur de l'appareil de mesures permet de suivre qualitativement l'apparition des ions tri iodure. | |
| observer le tracé progressif à l'écran des variations du pourcentage du flux lumineux F absorbé par le milieu de réaction. | |
| terminer éventuellement l'acquisition avant l'instant prévu (en cliquant-G sur l'icône 'Fin'), ou au contraire prolonger celle-ci si c évolue encore sensiblement. |
B. Variables transférées
1. dans le cas d'un spectrophotomètre
Ä
t, et A en cas d'acquisition avec un spectrophotomètreDans la fenêtre 'Graphiques' (menu Fenêtre/graphe Variables),
cliquer-D pour choisir 'Coordonnées' dans le menu contextuel, ou cliquer-G sur l'icône
correspondante ![]() pour vérifier qu'on a
bien:
pour vérifier qu'on a
bien:
| t en abscisses | |
| A en ordonnées (à gauche) |
2. dans le cas d'un colorimètreOn a ainsi la représentation graphique de A = f(t) qu'on peut déjà visualiser.
Ä
t, et U en cas d'acquisition avec un colorimètreDans la fenêtre 'Graphiques' (menu Fenêtre/graphe Variables),
cliquer-D pour choisir 'Coordonnées' dans le menu contextuel, ou cliquer-G sur l'icône
correspondante ![]() pour vérifier qu'on a
bien:
pour vérifier qu'on a
bien:
| t en abscisses | |
| U en ordonnées (à gauche) |
On a ainsi la représentation graphique de U = f(t) qu'on peut
déjà visualiser. On peut passer en coordonnées logarithmiques pour U: clic-G sur
l'icône ![]() pour choisir: 'Abscisse
/Graduation logarithmique' dans la liste déroulante. La représentation graphique
doit alors ressembler à l'opposé de l'absorbance puisque la définition de l'absorbance
introduite ici donnerait:
pour choisir: 'Abscisse
/Graduation logarithmique' dans la liste déroulante. La représentation graphique
doit alors ressembler à l'opposé de l'absorbance puisque la définition de l'absorbance
introduite ici donnerait:
y = log(U) = log(Uo)-A
Ä
NB: Penser à indiquer dans la ligne de commentaire sous la barre de menus principale (en haut à droite) les renseignements utiles sur la solution utilisée avant de sauver le fichier de données Regressi. V. Étude de la loi c = f(t)A. Représentation de A = f(l )
| Si l'absorbance n'a pas été mesurée directement lors de l'acquisition (cas d'un colorimètre), elle se déduit par sa définition. Revenir dans la fenêtre 'Grandeurs', onglet 'Expressions', et saisir directement dans une nouvelle ligne (touche 'Entrée' pour le saut de ligne, comme dans un traitement de texte) de ce 'mémo' : |
A = log(Uo/U)
pour créer la nouvelle grandeur A, et valider par la touche 'F2',
(ou 2 fois sur la touche 'Entrée', ou en cliquant-G sur l'icône
clignotante ![]() ); le résultat
apparaît alors dans l'onglet 'Variables'.
); le résultat
apparaît alors dans l'onglet 'Variables'.
| Dans la fenêtre 'Graphiques' (menu Fenêtre/graphe Variables), clic-D
pour choisir 'Coordonnées' dans le menu contextuel, ou clic-G sur l'icône
correspondante |
B. Représentation de c = f(t)
| Revenir dans la fenêtre 'Grandeurs', onglet 'Expressions', et saisir directement dans une nouvelle ligne de ce 'mémo': |
c = A /k
pour créer la nouvelle grandeur A, et valider par la touche 'F2',
(ou 2 fois sur la touche 'Entrée', ou
en cliquant-G sur l'icône clignotante ![]() );
le résultat apparaît alors dans l'onglet 'Variables'.
);
le résultat apparaît alors dans l'onglet 'Variables'.
| Dans la fenêtre 'Graphiques' (menu Fenêtre/graphe Variables), cliquer-D pour choisir
'Coordonnées' dans le menu contextuel, ou cliquer-G sur l'icône correspondante |
c en ordonnées, à gauche.
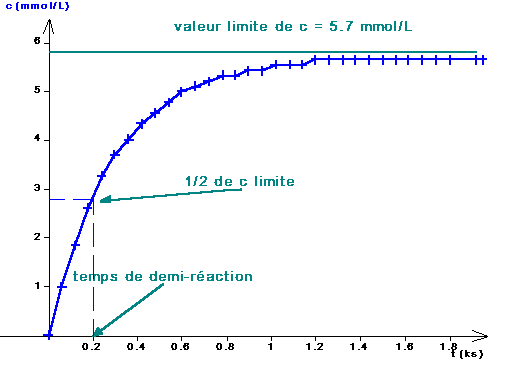
C. Valeur limite de la concentration; temps de demi réaction
|
charger le fichier Regressi: ioduoxy1.rw3
|
La valeur limite de c étant connue a priori, on peut l'ajouter sur le graphique sous forme d'asymptote à la courbe, par exemple avec le ‘curseur ligne’: choisir ce curseur dans la liste déroulante, laisser la touche majuscule enfoncée, et réaliser un ‘cliquer tirer’ d'un point à un autre : le segment apparu peut être édité (couleur, pointillés, etc.) par choix dans la boîte de dialogue qui s’ouvre lors d’un double-clic sur le segment. L’objet peut aussi être déplacé ultérieurement par cliquer-glisser. |
La détermination du temps de demi réaction peut être effectuée et commentée avec:
|
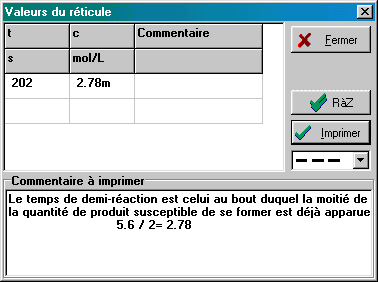 |
| Le curseur 'texte' permet alors d'annoter le graphique en y rajoutant une légende avec un cadre ou une flèche: choisir ce curseur (cliquer-G sur ce nom dans la liste déroulante des curseurs), cliquer-G sur le graphique à l'emplacement choisi pour le commentaire; saisir ce commentaire dans l'onglet 'texte' de la boîte qui s'ouvre automatiquement, et choisir entre les différentes présentations possibles dans l'onglet 'options' avant de valider. Ce commentaire (ou sa ligne de rappel) peut à tout moment être déplacé par cliquer-glisser du pointeur dessus, ou édité par double clic-G. |
Pour que l'asymptote tracée précédemment rencontre l'axe un peu plus
bas qu'à son extrémité supérieure, il faut remplacer le calcul automatique d'échelle
par un 'forçage' manuel: cliquer sur l'icône ![]() et imposer un maximum plus élevé pour
c; on peut ainsi ménager un
espace suffisant en haut du graphique pour ajouter un commentaire sur l'asymptote.
et imposer un maximum plus élevé pour
c; on peut ainsi ménager un
espace suffisant en haut du graphique pour ajouter un commentaire sur l'asymptote.
D. Détermination des vitesses de réaction
1. Vitesse instantanée de réaction
| On peut accéder à la vitesse instantanée de formation de l'ion tri iodure par la pente de la tangente à la courbe c(t). Choisir dans la liste déroulante le 'curseur tangente', et vérifier dans la boîte de dialogue qui s'ouvre que l'option 'méthode des tangentes' est bien décochée, puis valider; le curseur se déplace alors sous forme d'une tangente dont le point de contact est asservi aux mouvements du pointeur. La frappe de la touche 'Entrée' ou le double-clic G a pour effet de marquer la position courante de la tangente sur le graphique; plusieurs positions peuvent ainsi être marquées sur le même document. La même manœuvre effectuée sur une position déjà marquée permet de l'effacer. | 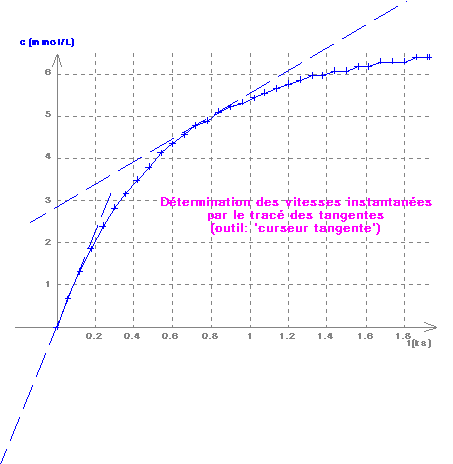 |
charger le fichier Regressi: ioduoxy2.rw3
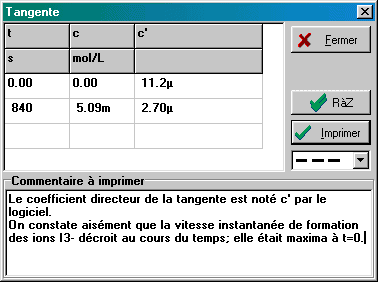 |
Simultanément, le logiciel calcule le coefficient directeur de la tangente pour chaque position marquée: on accède au tableau de valeurs correspondant par le menu contextuel (clic-D sur la fenêtre graphique) en choisissant 'Tableau tangentes'; la boîte de dialogue correspondante permet d'éditer l'aspect des tangentes (pointillés, etc.), la commande RAZ de cette boîte, ou du menu contextuel de la fenêtre graphique, permet de tout remettre à zéro. ! Attention:! les informations concernant les tangentes marquées (positions, valeurs, commentaires) ne sont pas sauvées avec le fichier dans la version actuelle de Regressi. |
On voit facilement lors de cette étude que:
| La vitesse de réaction décroît constamment en même temps que la concentration des réactants | |
| Cette vitesse est maximale au début, puis tend progressivement vers zéro. |
2. Vitesse moyenne de réaction
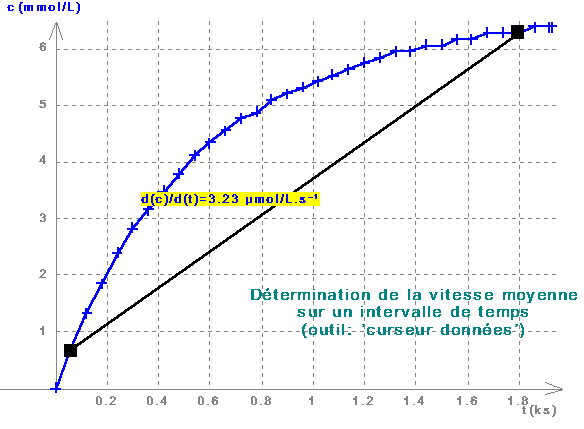
 |
Elle correspond à la pente de la sécante à la courbe c(t) sur un intervalle de temps quelconque. Choisir dans la liste déroulante le 'curseur données'. Il faut d'abord le paramétrer; en cochant 'pente' et 'écart', il affichera alors en bas de la fenêtre 'Graphique' ainsi que sur le graphe lui-même le coefficient directeur de la sécante à la courbe. Ce curseur est toujours asservi aux points expérimentaux: les deux extrémités du segment se déplacent par cliquer-glisser du pointeur sur chacune de ces extrémités. |
E. Modélisations éventuelles
(pour classes préparatoires seulement!)
| Rappel théorique: dans la mesure où les ions hydronium et iodure sont en excès, on peut écrire que la réaction est d'ordre partiel 1 par rapport à l'eau oxygénée: |
v = a*[H2O2]
ce qui donne, après intégration, pour la concentration du tri iodure formé:
c(t) = [H2O2]0*(1-exp(-a*t))
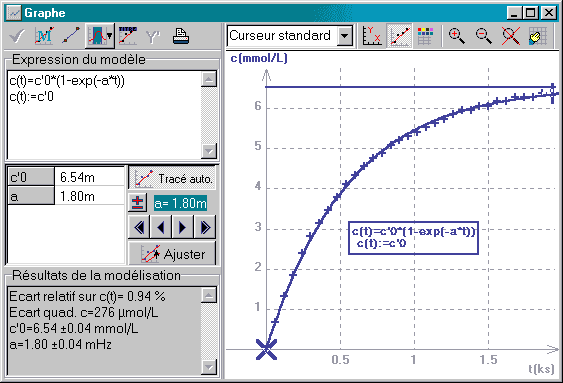
Dans la fenêtre 'Graphiques', cliquer-D pour choisir 'Modélisation' dans le menu
contextuel (raccourci clavier F9), ou cliquer-G sur l'icône correspondante ![]()
: un volet supplémentaire s'ouvre dans la partie gauche de la fenêtre. Saisir dans la zone "Expression du modèle" l'expression précédente sous la forme:
c(t) = c'0*(1-exp(-a*t))
On peut aussi utiliser en place de saisie manuelle des modèles
prédéfinis (accès par clic-G sur icône ![]() ).
).
| Valider par la touche 'F2', (ou 2 fois
sur la touche 'Entrée', ou en cliquant-G sur l'icône clignotante | |
| Dans le cas du modèle exponentiel, il faut parfois 'aider' le programme: indiquer dans
les cases où sont affichées les valeurs des paramètres (en dessous de l'équation du
modèle) une valeur très approximative, et demander à nouveau l'ajustage automatique.
S'il y a encore divergence dans ces conditions, il faut faire varier manuellement la
valeur de chaque paramètre en plaçant le curseur dans la case où figure cette valeur et
en cliquant sur les flèches NB : l'ajustement de la courbe modèle aux points expérimentaux se produit seulement si le bouton 'tracé auto' |
On obtient ainsi expérimentalement des valeurs pour la constante a de vitesse de réaction et pour la concentration initiale c'0 en eau oxygénée (réactif limitant).
| Pour obtenir automatiquement le tracé de l'asymptote, rester dans la fenêtre de modélisation, et saisir sur une nouvelle ligne, à la suite de l'équation du modèle: |
c(t):=c'0
en respectant précisément la syntaxe (le ':' avant le signe '='
indique a programme qu'il doit tracer le graphe de cette fonction avec la valeur issue de
la modélisation). Valider comme précédemment.
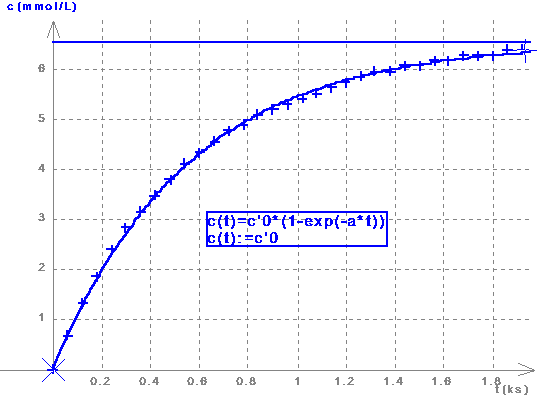
| Un clic-G sur l'icône 'Titre de la modélisation' |
VI. Suivi de cinétique par pesée avec une balance de précision
A. Principe
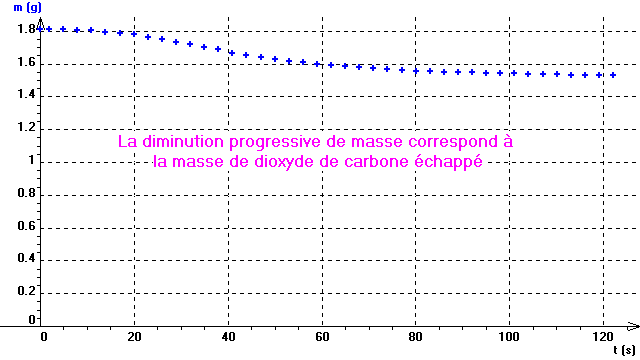
Il s'agit d'étudier la réaction accompagnant la dissolution d'un comprimé effervescent dans l'eau: (HCO3-)aq -----> (OH-)aq + CO2 et cela en suivant la variation de masse totale du milieu de réaction. Il s'agira en fait de la masse de dioxyde de carbone échappé du milieu de réaction. Cette masse étant relativement faible, il faut utiliser une balance de précision au 1/100 è gramme. Par exemple la balance Pioneer PA213 (réf Micrelec: M15G669), équipée d'une liaison série (=RS232) pour communiquer avec l'ordinateur.
|
 |
B. Mise en oeuvre
 |
Installer préalablement la version
de REGRESSI pour appareils RS 232 indispensable ici (voir cédérom
d'installation Regressi-Tépéor) .
Raccorder la balance au port Com (Com1 ou Com2) de l'ordinateur. |
1. Mise en oeuvre logicielle
Une fois la balance raccordée au port Com de l'ordinateur, lancer la version de REGRESSI pour appareils RS 232: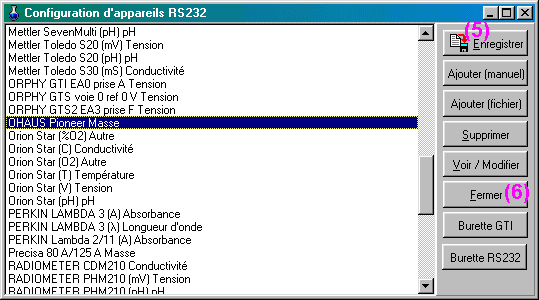
Si celle-ci ne s'y trouve pas, c'est que le fichier rs232.ini fourni avec le logiciel est trop ancien et doit être mis à jour. Procéder ainsi:
| menu Fichier/Gestion des appareils/Ajouter fichier: |
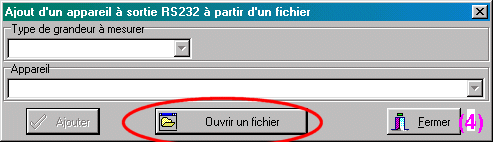
| cliquer sur le bouton "Ouvrir un fichier" pour
charger le fichier : |
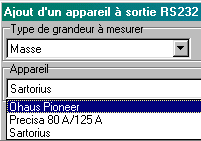
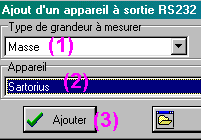
| (1) choisir
"masse" dans le type de grandeur à mesurer
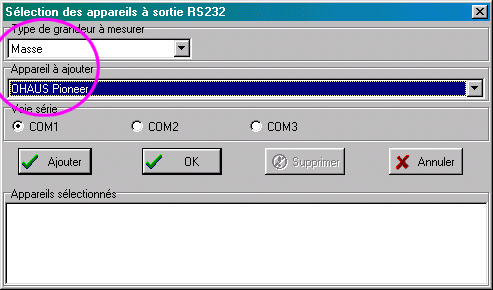
(2) choisir "Ohaus Pioneer" dans la liste déroulante des appareils (3) cliquer sur le bouton "Ajouter" (4) fermer le boite "ajout d'un appareil à sortie RS232" (5) enregistrer la configuration du nouvel appareil (6) fermer le boite de configuration |
|
|
 |
2. Mise en oeuvre matérielle
|
Le bécher étant placé sur la plateau de la balance, il s'agit de libérer le comprimé effervescent dans l'eau et de déclencher l'acquisition en même temps. |
3. Transfert vers Regressi et exploitation
retour sommaire chapitre en cours
![]()
I2 + I- ® I3-
(3) mais pas trop élevée pour tenir compte des limitations éventuelles du système de mesures: le logiciel du spectrophotomètre de Micrelec, par exemple, n'accepte pas de mesurer des absorbances supérieures à 1.9; les autres spectrophotomètres ne donnent souvent plus de mesure fiable au delà de A = 2
(4) ce choix est indifférent avec Orphy-GTI/GTI2/GTS2 puisque le calibre est choisi par voie logicielle quelque soit l'entrée choisie(5) une solution plus 'élégante' consiste à déclarer un nouveau capteur 'spectrophotomètre' dans le logiciel d'acquisition, ce qui permet d'en disposer automatiquement dans toute nouvelle session.
(6) Par exemple avec Win-GTS, cliquer-G sur l'icône 'Commencer' pour débuter les acquisitions. (7) si on a fait le choix d'une mesure toutes les 20 secondes; sinon, adapter… (8) les logiciels d'acquisition n'offrent pas tous cette possibilité (9) en remplaçant évidemment Uo par le résultat numérique de la mesure de "blanc" faite au § III C 3° (10) une seule frappe de la touche 'Entrée' réalise un saut de ligne, comme dans un traitement de texte(11) cependant, l'apparence des lignes affichées à l'écran de Regressi ne change pas si on a choisi l'option 'gras' pour le graphique; mais les copies faites dans le presse-papier seront bien actualisées
(12) la même manœuvre effectuée au même endroit aura pour effet d'effacer le marquage
(13) version au 1/9/99
(14) cette indication sera copiée avec le graphe dans le presse-papiers
(15) une seule frappe de la touche 'Entrée' réalise un saut de ligne.